Bochum, 16. Januar 2022
Bei frisch manifestiertem Typ-1-Diabetes von Erwachsenen sank nach Behandlung mit einem Antikörper gegen Interleukin (IL)-21 plus dem GLP-1-Rezeptoragonisten Liraglutid eine bei Studienbeginn vor 5 Jahren noch erhaltene stimulierte C-Peptidsekretion nur um 10% ab, weniger ab unter den anderen geprüften Therapieformen oder Plazebo. Nach Beendigung der Behandlung war dieser Effekt abgeklungen (1).
Methodik: Von 553 erwachsenen Patienten mit innerhalb der letzten 6 Monate manifestiertem Typ-1- Diabetes aus 17 Ländern an 94 Institutionen wurden 308 ausgewählt und je 77 zufallsverteilt vier Gruppen zugeordnet: Anti-IL-21 plus Liraglutid, Anti-IL-21 allein, Liraglutid allein sowie Plazebo. Alle erhielten diese Substanzen zusätzlich zu Insulin. Anti-IL-21 bzw. das Plazebo erhielten sie intravenös alle 6 Wochen, Liraglutid bzw. Plazebo spritzen die Patienten s.c. täglich selbst. Primäres Outcome waren die Veränderungen im mahlzeitenstimulierten C-Peptid bei Beendigung der Behandlung in der 54. Woche.
Ergebnisse:
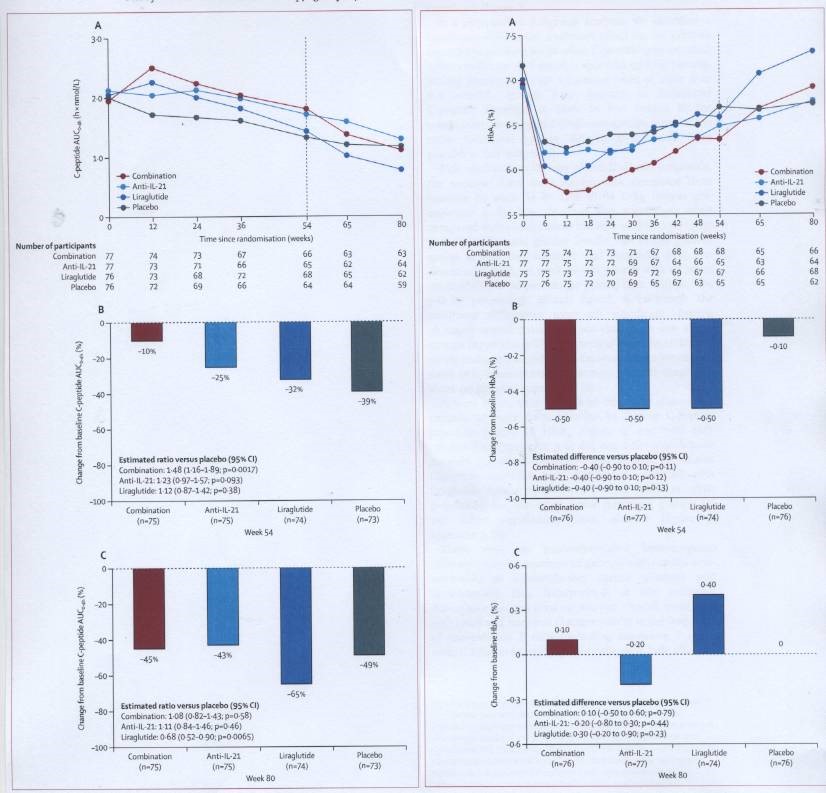
Abbildung 1 (die hier Fig. 2 und 4 aus Lit.1 zusammengestellt wiedergibt) zeigt die Resultate anschaulich: Links wird das mahlzeitenstimulierte C-Peptid dargestellt, rechts das das HbA1c. Die beiden oberen Graphiken (A) zeigen den zeitlichen Verlauf während der 54 Therapiewochen und während der anschließenden Nachbeobachtungsperiode bis zu 80 Wochen. Die beiden mittleren Graphiken (B) bilden die Befunde nach 54 Wochen bei Therapieende ab, und die unteren Graphiken (C) die Resultate nach insgesamt 80 Wochen.
Man erkennt, dass das stimulierte C-Peptid während der Therapie und auch in der Nachbeobachtungsperiode ab der 12. bzw. 24. Woche kontinuierlich abnahm. Bei Therapieende nach 54 Wochen war die Verringerung nach der Kombinationsbehandlung mit dem Anti-IL-21-Antikörper plus Liraglutid mit -10% am geringsten, unter Plazebo mit -39% am stärksten. Die Abnahme des HbA1c als key secundary outcome war zu Therapieende für alle aktiven Behandlungsgruppen im Vergleich zu Plazebo nicht signifikant unterschiedlich. In der 26-wöchigen Nachbeobachtungperiode stieg HbA1c in allen Gruppen wieder an, am stärksten in der Liraglutid-Gruppe (+0.4%). Die positiven Effekte auf die Betazellfunktion waren also nicht anhaltend, unter Liraglutid fand sich sogar eine Verschlechterung.
Nebenwirkungen: Am häufigsten wurden gastointestinale Effekte beobachtet. Es fand sich kein signifikanter Unterschied in den Hypoglykämie-Raten mit Ausnahme seltenerer Unterzuckerungen unter Liraglutid im Vergleich zu Plazebo. Es kam zu keinen Ketoazidosen.
Schlussfolgerung der Autoren: Die Studie mit der Kombination aus dem Anti-IL21-Antikörper plus Liraglutid ergab ähnliche Resultate wie die bisherigen Studien mit anderen Interventionen zur Beeinflussung des Krankheitsverlaufs bei Typ-1-Diabetes, jedoch mit einem besseren Sicherheitsprofil. Wirksamkeit und Sicherheit müssen jetzt in einem Phase-3 Programm untersucht werden (1).
Kommentar
Einleitend betonen S.A Long und C. Speake in einem Comment zu dieser Studie, dass bisher keine anerkannte Methode gebe, die Pathogenese des Typ-1-Diabetes zu modifizieren. Wenn auch generell bei Autoimmunkrankheiten der Verlauf durch Immunmodulation verlangsamt werden könne, so hätte sich auf Dauer die autoimmunologische Zelldestruktion nicht verhindern lassen. Dies gelte auch für den Typ-1-Diabetes. Und Liraglutid könnte sogar, wie sich in dieser Studie trotz anfänglicher Stimulation ergab, für das Überleben oder die Langzeitfunktion der Betazellen „harmful“ sein (2). Eine weitere Kommentatorin schrieb, die geprüfte Kombinationstherapie „shows promise“, ohne darauf näher einzugehen. (3). Bei uns in Deutschland forschen Anette Ziegler und ihre Mitarbeiter in München seit Jahrzehnten bei (Klein-)Kindern und Jugendlichen intensiv daran. Weltweit wurde bisher jedoch auf diesem Gebiet kein Durchbruch erzielt. Im DGE-Blog wurde mehrfach über dieses und das verwandte Thema der Verhinderung des Typ-1-Diabetes berichtet (4), auch über den Anti-CD-3 – Antikörper Teplizumab, welcher den Ausbruch eines Typ-1-Diabetes bei Verwandten mit hohem Risiko verzögerte (5).
In zwei von den National Institutes of Health und der Juvenile Diabetes Research Foundation gesponserten, doppelblinden, plazebokontrollierten Studien an neu manifestierten Typ-1-Diabetespatienten (Alter 6-45 Jahre) und noch erhaltener C-Peptidsekretion, eine mit Anakinra, einem Interleukin-1-Rezeptorantagonisten und eine zweite mit Canakinumab durch Blockade des Immunmediators Interleukin-1 über 9 bzw. 12 Monate erwiesen sich beide Medikamente als nicht wirksam (6). Vergleichsweise zu der hier referierten Studie war die Behandlungsdauer recht kurz. Es muss aber berücksichtigt werden, dass der in der oben besprochenen Studie eingesetzte Anti-IL-21-Antikörper weniger immunsuppressiv ist als die in diesen zwei Studien geprüften Substanzen.
Im von der Firma Novo Nordisk gesponserten Phase 3 -Studienprogramm wird sich zeigen müssen, ob nach sehr langer Behandlung mit der Kombination von Anti-Interleukin-21 plus Liraglutid die Betazellfunktion, erfasst als (Rest-)Sekretion von C-Peptid), dauerhaft auch nach Absetzen der Medikamente erhalten bleibt, und auch, ob über einen langen Zeitraum der Beeinflussung der humoralen und zellulären Immunabwehr die Sicherheit gewährleistet ist.
Helmut Schatz
Literatur
(1) Matthias von Herrath et al., for the Anti-IL-21 – Liraglutide Study Group: Anti-interleukin-21 antibody and liraglutide for the preservation of ß-cell function in adults with recent-onset type 1 diabetes: a randomised, double-blind, placebo-controlled, phase 2 trial.
Lancet Diabetes Endocrinol. 2021 April; 9(4):212-224
(2) S.A. Long, C. Speake: Combination therapy in recent-onset type 1 diabetes.
Lancet Diabetes Endocrinol. 2021 April; 9(4): 191-191
(3) S. Starling: New combination therapy shows promise for recent-onset type 1 diabetes mellitus.
Nat. Rev. Endocrinol. 2021 May; 17(5):257
(4) Kirsten P.Perrett et al.; Association of rotavirus vaccination with the incidence of type 1 diabetes in children.
JAMA Pediatr. 2019; 173(3): 280-202
(5) K.C. Herold et al., for the Type 1 Diabetes TrialNet Study Group: An Anti CD3 Antibody, Teplizumab, in Relatives at Risk for Type 1 Diabetes.
NEJM 2019. 381(7): 603-613
(6) A. Moran et al.: Interleukin-1 antagonisms in type 1 diabetes of recent onset: two multicentre, randomised, double-blind, placebo-controlled trials.
Lancet 2013; 381(9881): 1905-1015
Neueste Kommentare