Graz, 3. September 2020:
Testosteron-Undecanoat, welches über die Lymphbahnen des Darms und nicht wie Methyl-Testosteron über die Leber resorbiert wird und daher nicht hepatotoxisch ist, erwies sich in neuer oraler Galenik als gleich gut wirksam wie dermal als Gel appliziertes Testosteron. (1).
In einer Phase III – Studie wurden 222 hypogonade Männer im Alter von 18-65 Jahren in eine randomisierte, aktiv-kontrollierte open-label – Untersuchung eingeschlossen. 166 Patienten erhielten 3-4 Monate lang eine neue orale Präparation von Testosteron-Undecanoat (Jatenzo® der Firma Clarus Therapeutics) und 56 Männer Testosteron-Gel (Axiron®, Lilly, in Lizenz von Acrux). Die Dosis wurde anfangs titriert, um den von der US-Amerikanischen Arzneibehörde (FDA) geforderten Testosteron-Zielbereich im Serum von 300-1000 ng/ml (10-35 nmol/l) zu erreichen. Dieser sollte bei mindestens 75% der Probanden erreicht werden. Spitzenkonzentrationen sollten deutlich unter 1500 ng/dl (52 nmol/l) liegen.
Ergebnisse
Bei 87% der Patienten beider Gruppen traf dies zu. Der Mittelwert +/- Standardabweichung betrug mit oralem Testosteron-Undecanoat 403 +/- 128 ng/ml (~14 +/- 4 nmol/l), mit dem topischen Gel-Präparat 391 +/- 140 ng/ml (~14 +/- 5 nmol/l), dies bei nur 2x täglicher oralen Einnahme zum Frühstück und Abendessen. Die Resorption der neuen Hormonpräparation wurde zufolge einer ausgefeilten Galenik (s.u.) vom Fettgehalt der Nahrung nicht so beeinflusst wie die älteren oralen Testosteron-Undecanoat-Präparate (Andriol®, oder auch Jatenzo® in der bisherigen galenischen Zubereitung).
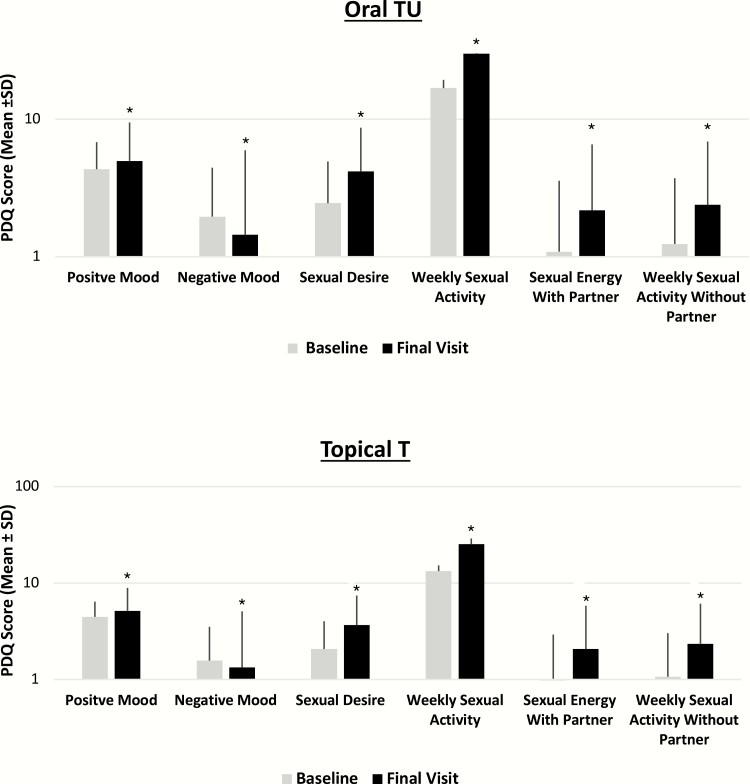
Klinisch wurden die Symptome des Hypogonadismus mit beiden Präparaten in etwa gleicher Weise signifikant gebessert (siehe Abbildung aus Lit.1). Die Sicherheitsparameter verhielten sich mit beiden Testosteron-Formulierungen ähnlich. Mit beiden Präparaten stieg der Hämatokrit im Referenzbereich an; mit der oralen Präparation überschritt er diesen in 3%, mit dem Gel vnicht. Der systolischen Blutdruck wurde unter dem oralen Präparat im Mittel um 3-5 mm Hg erhöht.
Abbildung (aus Lit.1):
Effects of oral TU (testosterone undecanoate) and topical T (testosterone) on mean change from baseline in Psychosexual Daily Questionnaire data at end of study (all T-treated patients).
*Statistically significant difference from baseline (P < 0.0001).
Diskussion
Testosteron kann über viele Wege substituiert werden: mit transdermalen Gelen und Lotionen, intramuskulären und subkutanen Injektionen, implantierten Pellets, dermalen Patches, intranasalen Gelen sowie oralen Kapseln und Tabletten. Bei jeder Applikationsart treten große oder kleinere Probleme und Nebenwirkungen auf. Methyliertes Testosteron zur oralen Applikation wurde bereits 1935 von Ruzika synthetisiert (siehe 2), um in der Leber nicht abgebaut zu werden. Es kann aber hepatotoxisch sein, von einer Cholestase bis hin zum Leberzellkarzinom, so dass es nicht mehr angewendet wird. Durch Veresterung mit Fettsäuren kann Testosteron aber über das Lymphsystem des Darmes aufgenommen werden und dadurch den Portalkreislauf umgehen. Die Resorption ist jedoch in hohem Maße vom Fettgehalt der Nahrung abhängig, so dass eine große Schwankungsbreite der Resorption und der Wirkung bestand. Mit den bisherigen galenischen Veränderungen gelang es meist nicht, einigermaßen stabile Serumspiegel zu erzielen, trotz 3-4x täglicher Einnahme bestand meist eine große Intra- und Intervariabilität bei den Patienten. Daher wurde eine neue Formulierung von Testosteron-Undecanoat entwickelt (1). Der hormonelle Wirkstoff ist von einer weichen Gelatinekapsel umhüllt und stellt eine Kombination mit Lipiden (langkettigen Fettsäuren (Oleinsäure u.a.), weiteren Lösungsvermittlern wie Borretschsamenöl, (reich an C-20 Fettsäuren), Pfefferminz-Öl und hydrophilen Tensiden als Surfactant (Castor-Öl) dar. Dies ermöglicht, dass das Testosteron-Undecanoat nach oraler Zufuhr mit der Nahrung auch dann recht konstant resorbiert werden kann, wenn diese nicht stark fetthaltig ist.
Die Galenik wird in diesem Blog deshalb so ausführlich dargestellt, da der Artikel wohl weniger von Pharmakologen und Pharmazeuten als von Medizinern gelesen werden dürfte. Dem Referenten (H.S.) wurde als Arzt beim Lesen der Arbeit wieder einmal bewusst, wie aufwendig und mühevoll es ist, bis ein Wirkstoff, den wir als Ärzte im beruflichen Alltag verwenden wie hier das Testosteron, in geeigneter Form hergestellt wird, damit er zugelassen wird, und dann noch weiter zu verbessern.
Helmut Schatz
Literatur
(1) Ronald S. Swerdloff et al.: A New Oral Testosterone Undecanoate Formulation Restores Testosterone to Normal Concentrations in Hypogonadal Men.
J Clin Endocrinol Metab Volume 105, Issue 8, August 2020. Dgaa238, https://doi.org/10.1210/clinem/dgaa238
(2) E. Nieschlag, S. Nieschlag: Endocrine History: the history of discovery, synthesis and development of testosterone for clinical use.
Eur J Endocrinol 2019.180(6):R 201-R212
Gibt es eventuell eine Vermutung, wie lange es noch dauern wird, bis diese neue Variante von Jatenzo auch in Europa bzw. speziell in Deutschland zugelassen wird? Für die Betroffenen würde das eine gute Alternative sein, wenn man Spritzen nicht mag sowie die Nachteile von Gel (Übertragung, Einwirkzeit) ersetzen könnte.
In den USA sicher noch Monate bis ein Jahr und länger, in Europa nach Beantragung dann wohl ebenso lang.
Danke für Ihre schnelle Antwort. Den Quellen der Endokrinologie in den USA zufolge, scheint es aber dort schon seit Juni 2020 zugelassen zu sein: https://www.endocrinologynetwork.com/view/the-latest-in-testosterone-replacement-therapy
Ich bin vo Zeitpunkt der Publikation der Phase III – Resutate ausgegangen. Da dauert es dann meist etwa so lange wie beschrieben. Darüber, dass das Präparat mittlerweile aber in den USA zugelassen ist, hatte mich keine Information. Offenbar war die jetzt publizierte Phase III-Studie schon länger abgeschlossen worden und wurde auch schon früher bei der FDA eingereicht. Danke für den Hinweis!